Misschien weet je het nog van je middelbare school natuurkunde: water wordt gas als het kookt. Maar… aan de andere kant lees je in het nieuws dat verdamping voor problemen zorgt. Hoe kan dat water nou verdampen? Wordt het water een gas zonder te koken? En hoe zit het dan met het tegenovergestelde, condensatie?
Water: een veelzijdig stofje
Water heeft 3 fases; ijs (vast), water (vloeibaar), en waterdamp (gas). Water komt in alle drie vormen (fases) voor. Verdampen betekent, de overgang van water naar waterdamp. Het tegenovergestelde is condenseren (van gas naar vloeistof). We hebben allemaal ervaring met smelten en bevriezen (stollen). Sublimeren en rijpen zijn wat minder bekend. Rijpen herkennen we veel beter als ik het heb over autoruiten krabben. Waterdamp (gas) is dan direct overgegaan naar ijs (vaste stof) op je autoruit. Bij sublimeren gaat ijs direct over in waterdamp, zonder dat het smelt. Dit gebeurt wel eens op een zeer droge en koude winterdag, dan verdwijnt zo de sneeuw. Sublimeren is wel heel traag.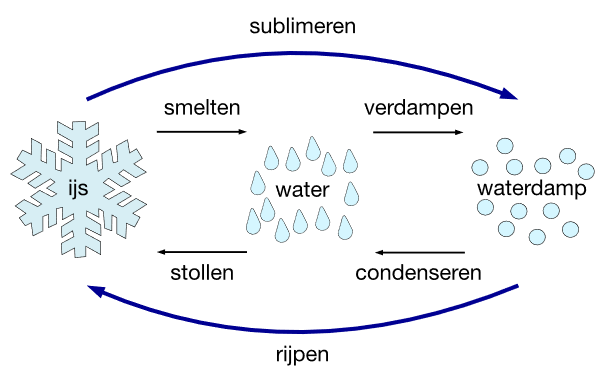
Bij water kennen we stollen beter als bevriezen. Rijpen herken je vast van het ruiten krabben. Bron: EllieBellie25 – Synkizz (CC BY-SA 4.0)
Het verschil tussen koken en verdampen
Heb je op een hete zomerdag net je vogelbadje aangevuld, kom je er een dag later achter dat je badje alweer leeg is. Hoe kan dat, waar is het water heen? Hebben de vogels zoveel gedronken? Is je badje lek? Nee, waarschijnlijk is je water verdampt.
Bij zowel koken als verdampen gaat water over in gas. In tegenstelling tot koken, kan vloeibaar water ook bij temperaturen lager dan 100 graden verdampen naar waterdamp (gas). Water kookt in Nederland op een temperatuur van 100 graden. Dan verandert water heel snel van vorm, het gaat snel over van vloeistof naar gas. Zelfs zo snel dat er hele belletjes uit het water omhoog borrelen. Bij verdamping kan het juist dagen of weken duren voordat iets verdampt is. Verdamping is dus een traag proces.
Als je een pannetje water laat koken stijgen de bellen ook altijd op vanaf de bodem van de pan, omdat het daar het warmste is. Verdamping vindt juist plaats vanaf het wateroppervlak, en niet vanaf de bodem.
Ten slotte is er nog een verschil in de energie. Bij koken moet je zelf energie toevoegen, zonder gas of elektriciteit warmt je pan niet op. Verdampen gaat juist vanzelf, je natte haar droogt gelukkig vanzelf op.
 Door de warmte van de zon verdampt het water. Eenmaal in de lucht condenseert het weer, waardoor wij het kunnen zien. Gelukkig verdampt het water, en is het wegdek niet aan het koken.
Door de warmte van de zon verdampt het water. Eenmaal in de lucht condenseert het weer, waardoor wij het kunnen zien. Gelukkig verdampt het water, en is het wegdek niet aan het koken.
Waterdamp: complete chaos
Watermoleculen zijn heel klein, en die hele kleine watermoleculen bewegen heel snel. In gas bewegen de watermoleculen heel snel, ze stuiteren alle kanten op, complete chaos. In water bewegen de watermoleculen wat minder snel, en in vaste vorm (ijs) zitten de moleculen aan elkaar vast en kunnen ze hoogstens en beetje trillen. De watermoleculen bewegen in gas en vloeistof zo snel, dat ze uit de bocht schieten, en zo “per ongeluk” de grens tussen water en lucht oversteken. Je ziet het niet, maar dit gebeurt altijd, er is altijd waterdamp dat vanzelf overgaat in water, en omgekeerd. Normaal is dit in evenwicht, er gaan evenveel moleculen uit het water als er terugkomen.
Er is pas sprake van verdamping als er meer moleculen de lucht in schieten, dan er moleculen terug het water inkomen. Het water verliest moleculen aan de lucht, en het water verdampt. Bij droge lucht zijn er überhaupt veel minder watermoleculen in de lucht, en hierdoor zijn er veel minder moleculen om terug naar het water te gaan. Het water verdampt dus sneller bij droge lucht.
 Verdamping: ontsnappen meer moleculen uit het water, dan er uit de lucht terugkomen.Is het buiten mistig en heel vochtig? Dan zit de lucht bomvol watermoleculen, en zullen er dus veel moleculen per ongeluk het water in stuiteren. Er komen dan haast evenveel watermoleculen terug het water in, als dat er uit het water. Er is bij vochtig weer amper verdamping, je kan dan heel lang wachten voordat het water uit je vogelbadje is verdampt.
Verdamping: ontsnappen meer moleculen uit het water, dan er uit de lucht terugkomen.Is het buiten mistig en heel vochtig? Dan zit de lucht bomvol watermoleculen, en zullen er dus veel moleculen per ongeluk het water in stuiteren. Er komen dan haast evenveel watermoleculen terug het water in, als dat er uit het water. Er is bij vochtig weer amper verdamping, je kan dan heel lang wachten voordat het water uit je vogelbadje is verdampt.
Koude rillingen door verdamping
Een overgang naar waterdamp kost energie. Bij koken komt die energie bijvoorbeeld van een gasvlam, bij verdamping koelt het dus af. Om dit te begrijpen moeten we eerst even weten dat snel bewegende moleculen een vloeistof opwarmen, en omgekeerd gaan de moleculen ook sneller bewegen als je het opwarmt. Bij verdamping schieten vooral de snelst bewegende moleculen weg, de achterblijvers zijn dus de tragere moleculen. De vloeistof koelt dan af, want de moleculen bewegen trager. Zo komt het dat verdamping voor afkoeling zorgt. Jij hebt dit al eens ervaren, denk maar aan de koude rillingen als je net uit de douche komt of hebt gezwommen. Dat komt doordat water verdampt van je natte huid, en hierdoor je huid afkoelt. Bij zweten gebruiken we verdamping juist. Je huid is te warm, en dus maak je je huid nat met zweet. Je natte zweet verdampt en koelt je huid weer af! Handig toch?
Beslagen douche en condensatie
We blijven nog even in de douche. Een beslagen douche is namelijk ook een mooi voorbeeld van condensatie. Als je lekker staat te douchen met warm water, dan is de lucht vochtig en warm. De warme en vochtige lucht komt een koude raam of douchecabine tegen. De waterdamp verandert dan recht voor je neus in vloeibaar water. Dit is hetzelfde proces als wolkenvorming. Een luchtbel met vochtige en warme lucht stijgt op, het wordt dan kouder (hoger in de lucht is het kouder). Dan vindt er condensatie plaats. Bij condensatie gaan de traagste moleculen als eerste over naar water, en warmt de waterdamp dus op, omdat de snelst bewegende moleculen over blijven. Bij condensatie komt dus warmte vrij. Misschien heb je bij aardrijkskunde geleerd dat warme lucht opstijgt. Door condensatie wordt de lucht dus nog iets warmer, waardoor het nog sneller stijgt en nog meer condenseert. Dit is een kettingreactie die uiteindelijk een bui veroorzaakt. Je leest in deze blogs meer over condensatie bij buien en bij mist.

Ook meer verdamping door warmte en wind
Warmte en wind veroorzaken ook meer verdamping. Als het water warm is, dan bewegen de watermoleculen sneller, en schieten ze dus makkelijk weg uit het water. Als de lucht warm is, dan is er in de lucht meer ruimte om water op te nemen (een lagere relatieve luchtvochtigheid). Hierdoor is er ook meer verdamping. Dit is beter uitgelegd in deze blogs over verdamping en relatieve luchtvochtigheid. Op een hete zomerdag kan er wel tot 7 millimeter water verdampen. Dit is evenveel water als er op een regenachtige dag in de winter kan vallen!

















